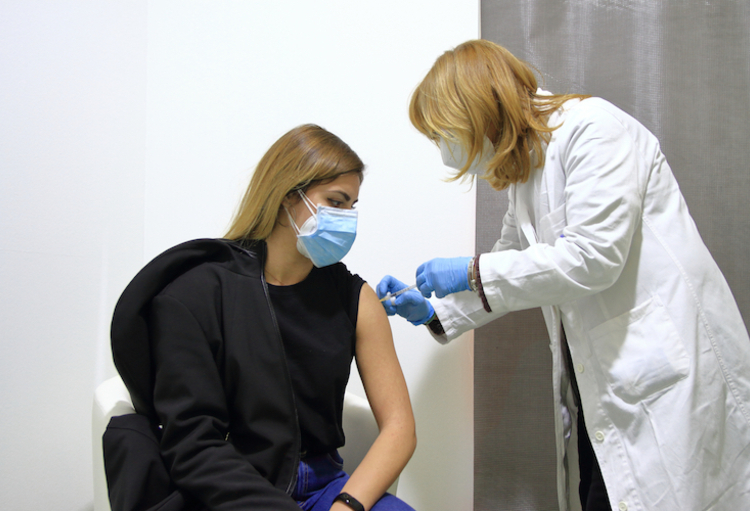
Le fait que la Commission européenne ait approuvé la distribution du vaccin Johnson & Johnson en Europe ne signifie pas que le développement en est terminé, explique Johan Van Hoof, patron de Janssen Vaccines. Des recherches complémentaires sont en cours, entre autres, sur la durabilité de la protection et les avantages possibles d'une seconde injection.
M. Van Hoof estime que le feu vert de la Commission européenne constitue un grand moment pour Johnson & Johnson. "Nous avions certainement espéré ce résultat. Sur la base de la confiance acquise, nous étions également prudemment optimistes quant à la suite de l'autorisation. Surtout au cours des deux dernières semaines, il y a e u un échange d'informations très intensif".
Le fait que le vaccin ait maintenant reçu le feu vert aux États-Unis et en Europe pourrait, selon Van Hoof, accélérer le processus d'autorisation dans d'autres parties du monde. "Les deux agences, MDA et EMA, sont des agences de premier plan, leur approbation donnera également confiance aux autres autorités du monde entier. Nous négocions à plusieurs endroits en utilisant le même principe de révision continue. J'attends plus d'approbations dans les jours et semaines à venir".
Bien qu'il y ait maintenant le feu vert pour commencer à fournir le vaccin, le travail du département de recherche et développement de Janssen Vaccines n'est pas terminé. "Ces approbations ont été très rapides, mais les agences s'attendent à ce que nous suivions les études en cours", déclare encore Johan Van Hoof. "Nous continuerons par exemple de surveiller les sujets de l'étude pour voir dans quelle mesure la protection de notre vaccin est durable".
Le vaccin Johnson & Johnson est le premier vaccin approuvé en Europe qui consiste en principe en une seule injection. "Mais nous étudions également l'efficacité d'une deuxième injection. Nous sommes très satisfaits des résultats avec une dose, mais par précaution - également en Belgique - nous avons commencé l'étude à propos de deux injections. Cela peut avoir une influence sur les formes plus douces de la maladie, ou étendre la protection."
Johan Van Hoof a enfin réaffirmé la conviction de Johnson & Johnson de pouvoir fournir 200 millions de doses en Europe tout au long de cette année. "Si tout se passe bien, nous pouvons commencer à livrer dans la deuxième quinzaine d'avril. Nous travaillons sur la production depuis plusieurs mois, mais cela reste un produit biotechnologique qui doit être soumis à de nombreux tests de contrôle. 99% du temps ces tests réussissent mais on ne sait jamais ce qui pourrait arriver".